Table of Contents
Toggle🔸 목표 요약
- 혈당 조절: HbA1c 6.5~7.0%, 공복 혈당 80~130 mg/dL
- 혈압 조절: 130/80 mmHg 미만
- 단백뇨 감소: UACR <30 mg/g, 50% 이상 감소
- 이상지질혈증 관리: LDL <70 mg/dL, 중성지방 <150 mg/dL
- 체중·식이 관리: 저염·저단백식, BMI 18.5~24.9 유지
- 신장 기능 모니터링: eGFR·크레아티닌·UACR 정기 검사
- 신장 독성 약물 주의: NSAIDs, 조영제 등 사용 최소화
1. 당뇨병 환자 3명 중 1명은 왜 신장병이 동반될까?
대한당뇨병학회(KDA)와 미국당뇨병학회(ADA) 통계에 따르면, **당뇨병 환자의 약 30~40%**가 신장합병증을 경험한다고 보고합니다. 흔히 “콩팥병”이라고 불리는 신장 질환은 단순히 수치상의 문제만이 아니라, 말기 신부전(ESRD)으로 진행되어 투석이나 신장 이식이 필요한 상태가 될 수 있기 때문에 매우 중요한 이슈입니다.
1) 만성 고혈당(Hyperglycemia)에 의한 직접 손상
- AGEs(Advanced Glycation End-products) 축적: 혈액 내 포도당이 세포 내·외 단백질과 결합해 만들어진 AGEs가 신장 혈관과 조직에 염증·섬유화를 일으킵니다.
- 사구체 고혈류(Hyperfiltration): 고혈당 상태가 이어지면 사구체 혈류가 과도하게 증가하여, 장기간 지속 시 오히려 사구체 손상을 가속화합니다.
이러한 기전은 DCCT(Diabetes Control and Complications Trial) 연구에서도 뒷받침됩니다. 연구에 따르면 엄격한 혈당 조절(HbA1c 평균 약 7%대 유지)이 당뇨병성 미세혈관 합병증, 특히 신장 합병증 발생 위험을 50% 이상 낮춘다고 보고됐습니다.
2) 고혈압(Hypertension)과의 상승작용
- 사구체 내압 증가: 고혈압은 작은 신장 혈관에 부담을 주어, 사구체 압력을 높이고 결과적으로 콩팥 기능을 떨어뜨립니다.
- RAAS(레닌-안지오텐신-알도스테론 시스템) 활성화: 당뇨병과 고혈압이 동시에 있을 때 RAAS가 과도하게 활성화되어 사구체·혈관 섬유화가 가속화됩니다.
임상적으로 ACE 억제제나 ARB(Angiotensin II Receptor Blocker)를 사용해 고혈압을 조절하면, 단백뇨가 줄고 신장 기능이 보존되는 연구가 다수 보고되었습니다. 예컨대 RENAAL 시험(레닌-안지오텐신 시스템 억제 관련 연구)에서는 당뇨병성 신장병 환자에게 로사르탄(losartan)을 투여했을 때 단백뇨가 유의미하게 감소했고, 신장 기능 보존 효과가 확인되었습니다.
3) 지방독성(Lipotoxicity)과 VEGF-B
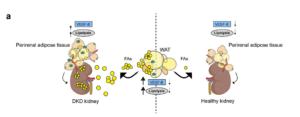
- VEGF-B의 역할: 비교적 최근에 주목받는 기전으로, VEGF-B가 백색 지방 조직(WAT)에서 지방산 방출을 유도하고 신장의 세포(특히 사구체나 세뇨관)에 과도한 지방 축적을 초래합니다.
- 신장 내 지방 축적: 이러한 지방산이 축적되면 미토콘드리아 기능 장애, 염증 반응 증가, 세포 손상 등 ‘지방독성’이 진행되어 신장 조직이 서서히 망가집니다.
실제 마우스 모델 연구에서 VEGF-B 신호를 차단한 결과, 신장 내 지방 축적과 손상이 크게 줄어들고, 신기능이 개선되었다는 점이 보고되었습니다. 이는 기존의 “혈당·혈압” 조절에 더해 “지방 축적 경로”도 중요함을 의미합니다.
4) 단백뇨(Proteinuria)
- 당뇨병성 사구체 변화로 인해 알부민 등 단백질이 소변으로 유출되면서, 단백뇨가 신장 손상을 악화시키는 또 다른 기전이 됩니다.
- 단백뇨 자체가 신장 세포에 독성을 부여해 염증·섬유화를 유발합니다.
신장 손상의 지표인 단백뇨는 치료 목표이자 예후 판단 기준입니다. UACR(요 알부민-크레아티닌 비율)이 30 mg/g 미만을 유지하거나, 이미 단백뇨가 있는 경우 이를 절반 이상 줄이는 것이 중요하다고 KDIGO(Kidney Disease: Improving Global Outcomes) 가이드라인에서 권고합니다.
2. 당뇨병성 신장 질환을 예방·관리하기 위한 7가지 핵심 목표
1) 혈당 조절
- 목표: HbA1c 6.5~7.0%, 공복 혈당 80~130 mg/dL
- 근거: DCCT 연구(제1형 당뇨병), UKPDS 연구(제2형 당뇨병) 등에서 혈당이 낮을수록 미세혈관 합병증 발생이 현저히 줄어듬이 확인되었습니다.
- 치료제 사례:
- SGLT2 억제제(empagliflozin, dapagliflozin 등): EMPA-REG OUTCOME 연구에서 심혈관계 및 신장 보호 효과 보고.
- GLP-1 수용체 작용제(liraglutide 등): LEADER 연구에서 심혈관 질환 및 일부 신장 합병증 감소 효과.
2) 혈압 조절
- 목표: 130/80 mmHg 미만
- 중요성: 혈압이 130/80 mmHg를 초과하면 사구체에 부담이 가중되고, 신장 기능이 빠르게 저하될 수 있습니다.
- 치료제 사례:
- ACE 억제제(예: enalapril), ARB(예: losartan): 단백뇨 감소 및 신장 보호 효과.
- CCB(칼슘 채널 차단제, amlodipine 등): 필요 시 병용.
3) 단백뇨 감소
- 목표: UACR <30 mg/g, 이미 단백뇨가 있는 경우 50% 이상 감소
- 근거: RENAAL, IDNT 등 대규모 임상 시험에서 단백뇨가 줄어드는 만큼 신장 기능 보전 효과가 커졌음이 관찰되었습니다.
- 치료제 사례:
- ACE/ARB, SGLT2 억제제, MRA(finerenone 등)
4) 이상지질혈증 관리
- 목표: LDL <70 mg/dL, 중성지방 <150 mg/dL
- 근거: 당뇨병 환자의 경우 죽상동맥경화 위험이 높아, 신장 혈관까지 손상될 수 있음.
- 치료제 사례:
- 스타틴(atorvastatin, rosuvastatin 등): 일부 연구에서 미세알부민뇨 개선.
- 피브레이트(fenofibrate): 단백뇨 감소에 기여(단, 신기능 저하 시 주의).
5) 체중 및 식이 조절
- 목표: BMI 18.5~24.9 유지, 저염식(하루 <2g 나트륨), 저단백식(0.8 g/kg/day)
- 사례: 대규모 전향적 연구(EPIC 연구 등)에서 정상 체중과 균형 잡힌 식이가 당뇨 합병증 발생을 유의미하게 낮춘다는 결과 보고.
- 의의: 비만은 인슐린 저항성을 악화시키고, 신장에 지방 축적을 촉진하는 요소가 됩니다.
6) 신장 기능 모니터링
- 항목: eGFR(추정 사구체 여과율), 혈중 크레아티닌, UACR
- 주기: 최소 연 1회 이상, 환자 상태에 따라 분기별로 혹은 더 자주 검사
- 의의: 초기에는 겉보기에 정상처럼 보여도, 미세알부민뇨나 eGFR 변화로 CKD가 시작될 수 있음을 조기 감지해야 함.
7) 신장 독성 약물 주의
- 예: NSAIDs(이부프로펜, 나프록센), 일부 항생제(아미노글리코사이드 계열), 조영제(CT나 MRI 시)
- 의의: 이미 손상된 신장에 더 큰 부담을 줄 수 있기 때문에, 대체 약물을 고려하거나 사용량·기간 최소화가 중요합니다.
3. 실제 환자 사례로 보는 통합 관리의 힘
-
사례 A: 50대 남성, 당뇨병 10년 차. 초기에는 HbA1c 8.5%, 혈압 145/90 mmHg, 미세알부민뇨(UACR 45 mg/g) 진단
- 관리 전략: SGLT2 억제제 + ACE 억제제 시작, 식이 조절(나트륨 줄이기), 스타틴 사용
- 결과: 1년 후 HbA1c 7.2%, 혈압 130/78 mmHg, UACR 25 mg/g로 감소. 신장 기능(eGFR)도 안정적으로 유지
-
사례 B: 60대 여성, 혈당은 비교적 잘 유지했으나(LDL 140 mg/dL) 이상지질혈증을 방치. 체중도 표준보다 10kg 초과
- 추가 위험: 고중성지방혈증으로 인해 당뇨병성 지방간, 신장 지방 축적 위험 증가
- 결과: 3년 후 경도의 신장 기능 저하(eGFR 60→50 mL/min/1.73㎡)와 단백뇨 진행
- 개선 방향: 스타틴 치료 및 식습관 개선(저염·저지방), 체중 감량 5kg 목표 설정 후 콩팥 기능 회복 추세
이처럼 체계적인 혈당·혈압·지질·체중·단백뇨 관리는 당뇨병성 신장 질환의 진행을 효과적으로 늦출 수 있습니다.
4. 앞으로의 전망: VEGF-B 연구와 새로운 치료
최근에는 VEGF-B 억제 전략을 통해 신장 내 지방 축적을 줄이고, 신기능을 보전하려는 전임상 연구가 활발합니다. 백색 지방 조직에서의 과도한 지방 분해(lipolysis)와 신장 지방 독성이 DKD를 가속화한다는 사실이 점차 분명해지고 있기 때문입니다.
- 의의: 기존 “혈당-혈압-단백뇨” 중심의 관리 외에도, 지방대사 경로까지 함께 개선할 수 있는 새로운 치료제가 나올 가능성이 열렸습니다.
- 한계: 아직 초기 단계 연구가 많아, 대규모 임상시험으로 이어진 사례는 제한적입니다.
결론: 종합적 접근이 관건!
당뇨병 환자의 약 1/3 정도가 신장병을 앓게 되는 것은 여러 기전이 복합적으로 작용하기 때문입니다. 고혈당, 고혈압, 단백뇨, 이상지질혈증, 지방독성 등 각각의 요소가 신장 손상을 동시다발적으로 유발합니다. 하지만 꾸준한 의학적 관리와 생활습관 개선을 통해 신장 기능 저하 속도를 상당 부분 늦출 수 있다는 점도 분명히 입증되었습니다.
- 혈당 조절은 기본 중의 기본입니다.
- 혈압 및 단백뇨 관리가 적절히 이뤄지면 신장 질환 진행이 눈에 띄게 줄어듭니다.
- 지방독성 문제를 해결하려면 적정 체중 유지와 지질 관리가 필수적입니다.
- 정기적인 신장 기능 검사로 변화를 모니터링하며, 이상 발견 시 빠르게 대처합니다.
- 신장 독성을 높이는 약물은 대체 의약품을 찾거나 사용을 최소화합니다.
또한, 향후에는 VEGF-B 표적 억제제가 개발되어, 신장 내 지방축적을 억제하는 혁신적 치료가 추가될 것으로 기대됩니다. 현재의 관리 원칙을 충실히 지키면서, 새로운 치료법에 대한 연구동향도 주목할 필요가 있겠습니다.
🔖 참고문헌 (References)
Vascular endothelial growth factor B-mediated fatty acid flux in the adipose-kidney axis contributes to lipotoxicity in diabetic kidney diseaseKidney International (2025) 107, 492–507;